第三针 FDA允许辉瑞 BioNTech 和 Moderna新冠疫苗针对免疫功能低下个体接种额外剂量
发布时间:2021-08-17
美国当地时间8月12日,美国FDA修改了辉瑞BioNTech COVID-19疫苗和Moderna COVID-19疫苗的紧急使用授权 (EUA),允许在某些免疫功能低下的个体中使用额外的剂量,特别是接受器官移植的患者或被诊断患有被认为具有同等免疫功能低下水平疾病的人。
“该国已进入另一波COVID-19大流行浪潮,FDA特别意识到免疫功能低下的人特别容易患上严重疾病。在对现有数据进行彻底审查后,FDA确定这个小而脆弱的群体可能会从第三剂疫苗中受益,”FDA Janet Woodcock 医学博士表示。FDA评估了在这些个体中使用第三剂辉瑞BioNTech和Moderna新冠疫苗的情况,并确定第三剂疫苗可能会增加对这些人群的保护。
目前,辉瑞BioNTech COVID-19疫苗被授权用于12岁及以上个人的紧急使用,Moderna COVID-19疫苗被授权用于18岁及以上个人的紧急使用。两种疫苗均分两次注射。辉瑞BioNTech COVID-19疫苗间隔三周注射,Moderna COVID-19疫苗间隔一个月注射。此次授权修订后,两款疫苗将被允许在对18岁或以上(辉瑞为12岁或以上)接种相同疫苗的两剂方案后至少28天给予额外或第三剂疫苗注射。
相关“第三针”的研究!
Moderna
Moderna在第二季度财报中公布的数据显示,在名为COVE的3期临床试验中,50μg的mRNA-1273作为增强疫苗显示出93%的功效,在第二剂给药后的六个月内,功效仍然持久,并正在开展100μg的增强疫苗临床试验。
来源:Moderna Q2财报
公司首席执行官史蒂芬·班塞尔(Stéphane Bancel)在财报发布的一份声明中说:“我们很高兴我们的COVID-19疫苗在六个月内显示出93%的持久效力,但我们认识到Delta变种是一个重要的新威胁,所以我们必须保持警惕。第三加强针可能是必要的,以使我们尽可能安全地度过北半球的冬季”。
辉瑞
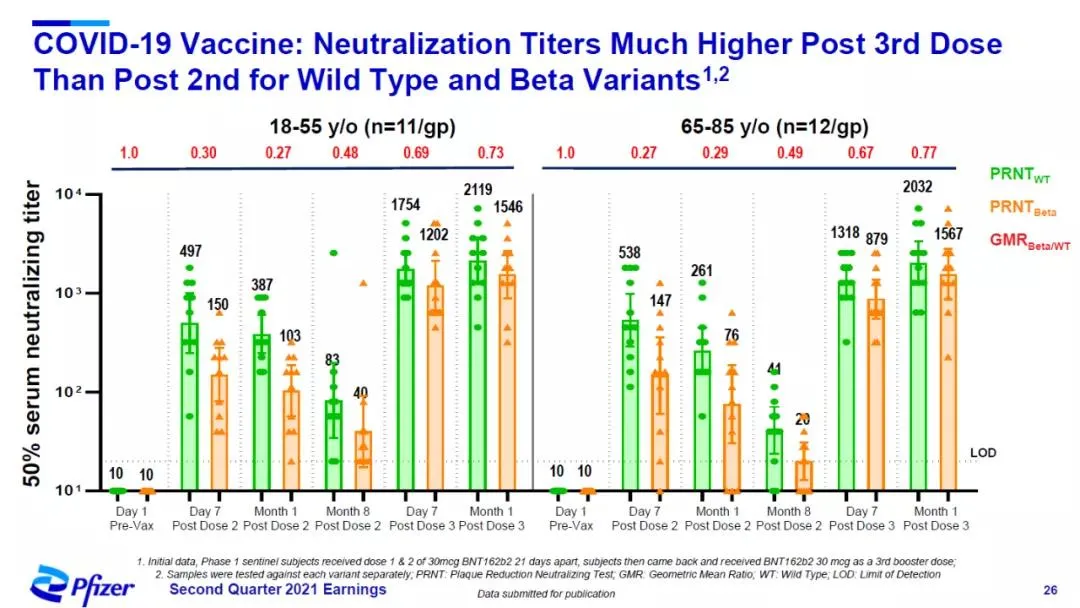
辉瑞在第二季度财报中公布了接种第三剂BNT162b2后血清中和活性数据。初步数据显示:
1.在接种第二剂6个月之后,接种第三剂增强疫苗表现出与此前一致的安全性特征;
2.针对野生型病毒,接种第三剂疫苗后中和抗体滴度比二针剂提高5-8倍;
3.针对Beta变种(B.1.351),接种第三剂疫苗后的中和抗体滴度比二针剂提高15-21倍;
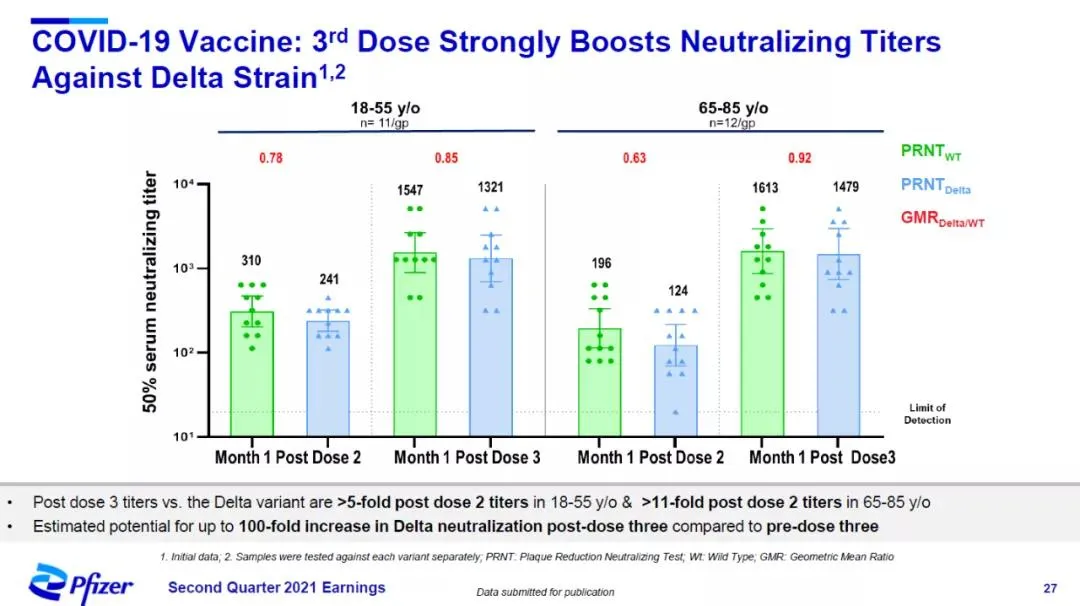
4.针对Delta变种,接种第三剂疫苗后的中和抗体滴度在18-55岁成人中提高5倍以上,在65-80岁老年人中提高11倍以上。
科兴生物
近期,江苏省疾病预防控制中心疫苗评价所联合复旦大学公共卫生学院、科兴控股生物技术有限公司(SINOVAC科兴)、复旦大学附属华山医院等多家单位,在预印本平台Medrxiv上共同公布了新冠疫苗第三针在18-59岁人群中的免疫有效性结果。
免疫原性分析显示:只打两针的情况下,半年后抗体水平会大幅降低:第2组在第194天时,抗体阳转率只剩16.9%,中和抗体GMT只剩4.1,第4组则分别为35.2%和6.7。接种第三剂后能迅速诱导强烈的免疫反应,中和抗体滴度显著提高:第1组第三针打完第28天,中和抗体GMT达到45.6,第2、3、4组分别为137.9、49.7、143.1。同时,数据显示第三剂与第二剂间隔时间越长,增长倍数越高。
来源:医谷 医学药学网